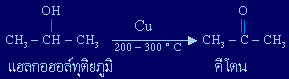เอมีนเป็นอนุพันธ์อินทรีย์ (organic derivatives) ของแอมโมเนีย (NH3) โดยมีหมู่ alkyl เข้ามาแทนที่hydrogen
เรียกชื่อ
ซึ่ง จะอยู่ภายในวงเล็บสําหรับตัวอย่างข้างล่างนี้ จะเรียกโดยการเรียกชื่อโซ่หรือวงแหวนหลักที่มีหมู่เอมีนต่ออยู่เป็น alkane จากนั้นตัด -e แล้วเติม –amineลงไปแทนเช่น
1.Primary amine
สำหรับ secondary และ tertiary amine จะใช้N-ตามด้วยชื่อหมู่แทนที่ที่ต่ออยู่กับไนโตรเจน (N-alkyl)เติมหน้าชึ่อหลักเดิมเช่น
2.Secondary amine
3.Tertiary amine
สมบัติ
2. เมื่อเปรียบเทียบจุดเดือดของแอลเคน เอมีน และแอลกอฮอล์ ที่มีมวลโมเลกุลใกล้เคียงกัน พบว่าเอมีนมีจุดเดือดสูงกว่าแอลเคน แต่ต่ำกว่าแอลกอฮอล์ เนื่องจากแอลเคนเป็นโมเลกุลไม่มีขั้ว แต่เอมีนเป็นโมเลกุลมีขั้ว จึงมีทั้งแรงลอนดอนและแรงดึงดูดระหว่างขั้ว นอกจากนี้เอมีนยังสามารถเกิดพันธะไฮโดรเจนได้ด้วย สำหรับเอมีนกับแอลกอฮอล์เป็นโมเลกุลที่มีขั้วทั้งคู่ แต่สภาพขั้วของเอมีนอ่อนกว่าแอลกอฮอล์ แรงยึดเหนี่ยวระหว่างโมเลกุลจึงน้อยกว่าแอลกอฮอล์
จุดเดือด แอลกอฮอล์ > เอมีน > แอลเคน
ปฏิกิริยา
primary ---> secondary
sencondary ---> tertiary